Pentacyanocyclopentadien
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Allgemeines | ||||||||||
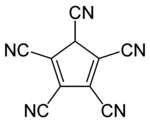
| Name | Pentacyanocyclopentadien | |||||||||
| Summenformel | C10HN5 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 191,1 g·mol−1 | |||||||||
| pKS-Wert | < −11[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Pentacyanocyclopentadien ist eine cyclische Kohlenstoffverbindung. Sie enthält fünf Cyanogruppen (–CN) und zwei Doppelbindungen im Molekül, daher gehört sie zu den Cycloalkadienen. Die Verbindung ist eine extrem starke Säure, sodass sie nur als Salz mit einem Cyclopentadienid-Ion isoliert werden kann.
Herstellung
Pentacyanocyclopentadien kann ausgehend von Cyclopentadien durch schrittweise Einführung der Cyanogruppen gewonnen werden. Die ersten drei Schritte erfolgen dabei durch Deprotonierung mit Natriumhydrid und Umsetzung mit Chlorcyan. Die vierte und fünfte Gruppe können durch eine Friedel-Crafts-Reaktion mit Chlorcyan sowie Aluminiumchlorid als Katalysator eingefügt werden. Wegen ihrer extrem hohen Acidität kann die Verbindung nur als Anion in Form eines Salzes isoliert werden.[3]
Eigenschaften
Die Tetraalkylammonium-Salze des Cyclopentadiens sind im Allgemeinen weiße Feststoffe.[3] Die Acidität der Verbindung beruht analog zu der Stammverbindung Cyclopentadien auf der Ausbildung eines aromatischen Systems im entsprechenden Anion. Verstärkt wird Stabilisierung durch den elektronenziehenden Effekt der Cyanogruppen.[4]

- Nach Deprotonierung ist das Anion von Pentacyanocyclopentadien mesomeristabilisiert.
So besitzt es einen extrem niedrigen pKs-Wert von <−11.[3][1] Damit ist es eine deutlich stärkere Säure als selbst Perchlorsäure.[3]
Einzelnachweise
- ↑ a b Jonathan Clayden, Nick Greeves, Stuart G. Warren: Organic Chemistry. 2. Auflage. Oxford University Press, Oxford 2012, ISBN 978-0-19-927029-3.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c d O. W. Webster: Polycyanation. The Reaction of Cyanogen Chloride, Cyclopentadiene, and Sodium Hydride. In: Journal of the American Chemical Society. Band 88, Nr. 13, Juli 1966, S. 3046–3050, doi:10.1021/ja00965a028.
- ↑ Robert Vianello, Joel F. Liebman, Zvonimir B. Maksić: In Search of Ultrastrong Brønsted Neutral Organic Superacids: A DFT Study on Some Cyclopentadiene Derivatives. In: Chemistry – A European Journal. Band 10, Nr. 22, 19. November 2004, S. 5751–5760, doi:10.1002/chem.200400337.









