Acide nitrosylsulfurique
| Acide nitrosylsulfurique | |||
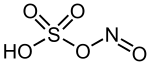 Structure de l'acide nitrosylsulfurique | |||
| Identification | |||
|---|---|---|---|
| Synonymes | acide nitrosulfonique, | ||
| No CAS | 7782-78-7 | ||
| No ECHA | 100.029.058 | ||
| No CE | 231-964-2 | ||
| PubChem | 82157 | ||
| SMILES | N(=O)OS(=O)(=O)O PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/HNO5S/c2-1-6-7(3,4)5/h(H,3,4,5) Std. InChIKey : VQTGUFBGYOIUFS-UHFFFAOYSA-N | ||
| Apparence | cristaux incolores à l'odeur piquante | ||
| Propriétés chimiques | |||
| Formule | HNO5S [Isomères] | ||
| Masse molaire[1] | 127,077 ± 0,007 g/mol H 0,79 %, N 11,02 %, O 62,95 %, S 25,23 %, | ||
| Propriétés physiques | |||
| T° fusion | décomposition à 73,5 °C[2] | ||
| Précautions | |||
| SGH[3] | |||
  Danger H272 : Peut aggraver un incendie ; comburant H290 : Peut être corrosif pour les métaux H314 : Provoque de graves brûlures de la peau et des lésions oculaires H330 : Mortel par inhalation EUH014 : Réagit violemment au contact de l'eau EUH029 : Au contact de l'eau, dégage des gaz toxiques P220 : Tenir/stocker à l’écart des vêtements/…/matières combustibles P260 : Ne pas respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P284 : Porter un équipement de protection respiratoire. P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin. P301+P330+P331 : En cas d'ingestion : rincer la bouche. NE PAS faire vomir. P304+P340 : En cas d'inhalation : transporter la victime à l’extérieur et la maintenir au repos dans une position où elle peut confortablement respirer. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P402+P404 : Stocker dans un endroit sec. Stocker dans un récipient fermé. | |||
| Transport[3] | |||
Code Kemler : X80 : matière corrosive ou présentant un degré mineur de corrosivité réagissant dangereusement avec l'eau) Numéro ONU : 3456 : HYDROGÉNOSULFATE DE NITROSYLE SOLIDE Classe : 8 Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage II : matières moyennement dangereuses ; | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
L’acide nitrosylsulfurique est un composé chimique de formule (NO)HSO4. Il s'agit d'un solide incolore cristallisé utilisé dans l'industrie pour produire le caprolactame (CH2)5C(O)NH[4], précurseur du nylon 6.
L'acide nitrosylsulfurique se forme lorsqu'on fait réagir des oxydes d'azote avec de l'acide sulfurique H2SO4 concentré, par exemple comme sous-produit du procédé des chambres de plomb. Cette molécule peut également être vue comme l'anhydride d'acide sulfurique et d'acide nitreux HNO2, et peut être obtenue en introduisant du dioxyde de soufre SO2 dans de l'acide nitrique HNO3[5].
- HNO2 + H2SO4 → (NO)HSO4 + H2O.
- SO2 + HNO3 → (NO)HSO4.
On utilise l'acide nitrosylsulfurique industriellement pour produire le caprolactame, ainsi que des colorants et des pesticides. Il est également utilisé en chimie organique pour préparer des sels de diazonium à partir d'amines ; les réactifs apportant le groupe nitroso NO peuvent alors être le tétrafluoroborate de nitrosyle (NO)BF4 ou le chlorure de nitrosyle NOCl par exemple.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a et b Entrée « Nitrosylsulfuric acid » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 26 décembre 2014 (JavaScript nécessaire)
- ↑ a b et c Fiche Sigma-Aldrich du composé Nitrosylsulfuric acid solution 40 wt. % in sulfuric acid, consultée le 26 décembre 2014.
- ↑ (en) Josef Ritz, Hugo Fuchs, Heinz Kieczka et William C. Moran, « Caprolactam », Ullmann's Encyclopedia of Industrial Chemistry, (DOI 10.1002/14356007.a05_031, lire en ligne)
- ↑ (en) George H. Coleman, Gerald A. Lillis, Gilbert E. Goheen, C. V. Herrmann et H. S. Booth, « Nitrosyl Chloride », Inorganic Syntheses, vol. 1, (DOI 10.1002/9780470132326.ch20, lire en ligne)
Articles connexes
v · m | |
|---|---|
|
 Portail de la chimie
Portail de la chimie













