Acide phosphoénolpyruvique

Pour les articles homonymes, voir PEP.
| Acide phosphoénolpyruvique | |
 Structure de l'acide phosphoénolpyruvique | |
| Identification | |
|---|---|
| Nom UICPA | Acide 2-phosphonooxyprop-2-ènoïque |
| No CAS | 138-08-9 |
| No ECHA | 100.004.830 |
| No CE | 205-312-2 |
| PubChem | 1005 |
| ChEBI | 44897 |
| SMILES | C=C(C(=O)O)OP(=O)(O)O PubChem, vue 3D |
| InChI | InChI : vue 3D InChI=1/C3H5O6P/c1-2(3(4)5)9-10(6,7)8/h1H2,(H,4,5)(H2,6,7,8)/f/h4,6-7H InChIKey : DTBNBXWJWCWCIK-HPEAKAIJCD Std. InChI : vue 3D InChI=1S/C3H5O6P/c1-2(3(4)5)9-10(6,7)8/h1H2,(H,4,5)(H2,6,7,8) Std. InChIKey : DTBNBXWJWCWCIK-UHFFFAOYSA-N |
| Propriétés chimiques | |
| Formule | C3H5O6P [Isomères] |
| Masse molaire[1] | 168,042 ± 0,004 6 g/mol C 21,44 %, H 3 %, O 57,13 %, P 18,43 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier  | |
L’acide phosphoénolpyruvique — ou phosphoénolpyruvate sous forme déprotonée, abrégée en PEP — est un composé organique important en biochimie, en raison notamment de son groupe phosphate à haut potentiel de transfert (ΔG°' = −61,9 kJ mol−1, valeur la plus élevée trouvée chez les êtres vivants). Il intervient par conséquent comme métabolite de la glycolyse en relation avec la chaîne respiratoire, fournissant l'énergie nécessaire à la phosphorylation d'une molécule d'ADP en ATP. Il intervient également comme accepteur de CO2 hydraté (HCO3-) chez les plantes au métabolisme C4 ou CAM, pour former l'oxaloacétate, dans une réaction catalysée par la phosphoénolpyruvate carboxylase.
Rôle dans la glycolyse
Pour un article plus général, voir glycolyse.
'Biosynthèse' 'Dégradation' 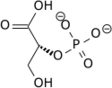
H2O + 

+ ADP + H+ → ATP + 
2PG PEP PEP Pyruvate Énolase (phosphopyruvate hydratase) – EC 4.2.1.11 Pyruvate kinase – EC 2.7.1.40
Biosynthèse
Le 2-phospho-D-glycérate (2PG) produit au cours de la glycolyse est déshydraté par une lyase, l’énolase (ou phosphopyruvate hydratase), pour former le phosphoénolpyruvate (PEP). Un cation Mg2+ est requis comme « catalyseur » de la réaction de déshydratation, tandis qu'un second Mg2+ intervient avec un rôle « conformationnel » en coordination avec le groupe carboxyle du 2PG.
Dégradation
Le groupe phosphate à haut potentiel de transfert (ΔG°' = −61,9 kJ mol−1) du PEP permet la phosphorylation d'une molécule d'ADP en ATP par la pyruvate kinase. Un cation Mg2+ est nécessaire à cette réaction comme cofacteur.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
Voir aussi
v · m | |
|---|---|
| Voie du shikimate |
|
 Portail de la biochimie
Portail de la biochimie  Portail de la chimie
Portail de la chimie














