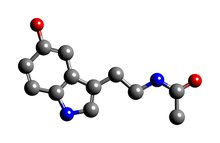
N-아세틸세로토닌
 | |
 | |
| 이름 | |
|---|---|
| 우선명 (PIN) N-[2-(5-Hydroxy-1H-indol-3-yl)ethyl]acetamide | |
| 별칭 N-Acetyl-5-hydroxytryptamine N-Acetyl-5-HT | |
| 식별자 | |
| |
3D 모델 (JSmol) |
|
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.013.560 |
IUPHAR/BPS |
|
| MeSH | N-Acetylserotonin N-Acetylserotonin |
PubChem CID |
|
| UNII |
|
CompTox Dashboard (EPA) |
|
| |
SMILES
| |
| 성질 | |
| C12H14N2O2 | |
| 몰 질량 | 218.256 g·mol−1 |
| 밀도 | 1.268 g/mL |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.  아니오 확인 (관련 정보 아니오 확인 (관련 정보  예 예 아니오 ?) 아니오 ?) 정보상자 각주 | |
N-아세틸세로토닌(영어: N-acetylserotonin, NAS) 또는 노르멜라토닌(영어: normelatonin)은 세로토닌으로부터 멜라토닌을 내인성으로 생성하는 과정에서의 자연적으로 생성되는 화학 전구체 및 대사 중간생성물이다.[1][2] N-아세틸세로토닌은 멜라토닌 수용체 작용제, 트로포마이오신 수용체 키네이스 B(TrkB) 수용체의 작용제로서 작용하고 항산화 효과를 갖는 것을 포함하여 그 자체로 생리활성을 가지고 있다.
생리 기능
멜라토닌과 마찬가지로 N-아세틸세로토닌은 멜라토닌 수용체인 멜라토닌 수용체 1A, 멜라토닌 수용체 1B, 멜라토닌 수용체 1C의 작용제이며, 신경전달물질로 간주될 수 있다.[3][4][5][6] 또한 N-아세틸세로토닌은 세로토닌과 멜라토닌이 없는 뇌의 일부 영역에 분포되어 있어 멜라토닌의 합성 과정에서 전구체로 작용하는 것 뿐만 아니라 고유의 중심적인 역할을 가질 수 있음을 시사한다.[3] N-아세틸세로토닌은 항우울제, 신경영양 효과 및 인지강화 효과를 가지고 있는 것으로 알려져 있으며,[7][8] 노화와 관련된 인지력 감퇴 및 우울증의 치료를 위한 표적으로 제안되었다.[8]
트로포마이오신 수용체 키네이스 B(TrkB) 수용체
N-아세틸세로토닌은 강력한 트로포마이오신 수용체 키네이스 B(TrkB) 수용체의 작용제로 작용하는 반면, 세로토닌과 멜라토닌은 그렇지 않다.[3] 쥐에 대한 N-아세틸세로토닌의 아만성 및 만성 투여는 신경 전구세포(NPC)의 증식을 유도하고, TrkB의 차단은 이러한 효과가 TrkB 의존적임을 시사한다.[9] N-아세틸세로토닌은 또한 수면이 부족한 생쥐에서 N-아세틸세로토닌을 크게 증가시키는 것으로 밝혀졌다.[9] N-아세틸세로토닌의 항우울제 및 신경영양 효과는 부분적으로 TrkB 수용체의 작용체로서의 역할에 기인한다고 생각된다.[7]
항산화 특성
N-아세틸세로토닌은 강력한 항산화제로 역할을 하며, 항산화제로서의 N-아세틸세로토닌의 효과는 사용된 실험 모델에 따라 다른 것으로 밝혀졌으며, 산화적 손상으로부터 호호하는 데 멜라토닌보다 5배~20배 더 높은 효과가 있는 것으로 설명되었다.[10] N-아세틸세로토닌은 마이크로솜 및 미토콘드리아에서 지질 과산화로부터 세포소기관을 보호하는 것으로 나타났다.[11] N-아세틸세로토닌은 또한 말초 혈액 림프구에서 활성산소의 수준을 낮추고 t-뷰틸화 하이드로퍼옥사이드 유도 활성산소 및 다이아마이드 유도 활성산소에 대한 항산화 효과를 나타내는 것으로 보고되었다.[12] N-아세틸세로토닌은 또한 산화 질소 생성효소를 저해하는 것으로 관찰되었다.[13]
항염증 효과
N-아세틸세로토닌은 항염증 효과가 있는 것으로 보고되었다. N-아세틸세로토닌은 분화된 THP-1 유래 사람 단핵구에서 전염증성 사이토카인 종양괴사인자-α(TNF-α)의 지질다당류 자극 생산을 억제하는 것으로 나타났다.[14]
기타 특성
N-아세틸세로토닌은 선택적 세로토닌 재흡수 저해제(SSRI) 및 모노아민 산화효소 저해제(MAOI)의 항우울제 효과에 역할을 할 수 있다.[3] 선택적 세로토닌 재흡수 저해제(SSRI)인 플루옥세틴과 모노아민 산화효소 A 저해제인 클로르길린은 세로토닌 작동성 기작을 통해 간접적으로 아르알킬아민 N-아세틸트랜스퍼레이스(AANAT)를 상향 조절하여 만성 투여 후 N-아세틸세로토닌의 수준을 증가시키며, 이는 항우울제 효과와 관련이 있다.[3][15] 게다가 빛에 노출되는 것은 N-아세틸세로토닌의 합성을 억제하고, 모노아민 산화효소 저해제(MAOI)의 항우울제 효과를 감소시킨다.[3] 또한, 아르알킬아민 N-아세틸트랜스퍼레이스(AANAT) 유전자제거 생쥐는 동물에 대한 우울증 실험에서 대조군 쥐에 비해 상당히 큰 부동시간을 나타낸다.[3] 이러한 데이터는 기분 조절 및 항우울제로 인한 치료 효과에서 N-아세틸세로토닌의 잠재적인 역할을 지원한다.
N-아세틸세로토닌은 현재 확인되지 않는 메커니즘에 의한 모노아민 산화효소 저해제(MAOI)의 임상 치료에서 보이는 기립성 저혈압의 원인이 될 수 있다.[15][16] N-아세틸세로토닌은 설치류에서 혈압을 낮추고, 솔방울샘 절제(솔방울샘은 N-아세틸세로토닌 및 멜라토닌 합성의 주요 부위임)는 클로르길린의 저혈압 효과를 없앤다.[15][16]
생화학
N-아세틸세로토닌은 아르알킬아민 N-아세틸트랜스퍼레이스(AANAT)에 의해 세로토닌으로부터 생성되고, 아세틸세로토닌 O-메틸트랜스퍼레이스(ASMT)에 의해 멜라토닌으로 전환된다.
N-아세틸세로토닌은 세로토닌과 달리 혈액뇌장벽을 통과할 수 있다.[17]
같이 보기
각주
- ↑ AXELROD J, WEISSBACH H (April 1960). “Enzymatic O-methylation of N-acetylserotonin to melatonin”. 《Science》 131 (3409): 1312. doi:10.1126/science.131.3409.1312. PMID 13795316.
- ↑ WEISSBACH H, REDFIELD BG, AXELROD J (September 1960). “Biosynthesis of melatonin: enzymic conversion of serotonin to N-acetylserotonin”. 《Biochimica et Biophysica Acta》 43: 352–3. doi:10.1016/0006-3002(60)90453-4. PMID 13784117.
- ↑ 가 나 다 라 마 바 사 Jang SW, Liu X, Pradoldej S, 외. (February 2010). “N-acetylserotonin activates TrkB receptor in a circadian rhythm”. 《Proceedings of the National Academy of Sciences of the United States of America》 107 (8): 3876–81. doi:10.1073/pnas.0912531107. PMC 2840510. PMID 20133677.
- ↑ Zhao H, Poon AM, Pang SF (March 2000). “Pharmacological characterization, molecular subtyping, and autoradiographic localization of putative melatonin receptors in uterine endometrium of estrous rats”. 《Life Sciences》 66 (17): 1581–91. doi:10.1016/S0024-3205(00)00478-1. PMID 11261588.
- ↑ Nonno R, Pannacci M, Lucini V, Angeloni D, Fraschini F, Stankov BM (July 1999). “Ligand efficacy and potency at recombinant human MT2 melatonin receptors: evidence for agonist activity of some mt1-antagonists”. 《British Journal of Pharmacology》 127 (5): 1288–94. doi:10.1038/sj.bjp.0702658. PMC 1566130. PMID 10455277.
- ↑ Paul P, Lahaye C, Delagrange P, Nicolas JP, Canet E, Boutin JA (July 1999). “Characterization of 2-[125I]iodomelatonin binding sites in Syrian hamster peripheral organs”. 《The Journal of Pharmacology and Experimental Therapeutics》 290 (1): 334–40. PMID 10381796. 2019년 12월 15일에 원본 문서에서 보존된 문서. 2020년 4월 13일에 확인함.
- ↑ 가 나 Tosini G., Ye K. & Iuvone PM (2012). “Neuroprotection, neurogenesis, and the sleepy brain”. 《Neuroscientist》 18 (6): 645–653. doi:10.1177/1073858412446634. PMC 3422380. PMID 22585341.
- ↑ 가 나 Oxenkrug G. & Ratner R. (2012). “N-acetylserotonin and aging-associated cognitive impairment and depression”. 《Aging Dis》 3 (4): 330–338.
- ↑ 가 나 Sompol P.; Liu X.; Baba K.; Paul KN.; Tosini G.; Iuvone PM.; Ye K. (2011). “N-acetylserotonin promotes hippocampal neuroprogenitor cell proliferation in sleep-deprived mice”. 《Proc. Natl. Acad. Sci. U.S.A.》 108 (21): 8844–9. doi:10.1073/pnas.1105114108. PMC 3102377. PMID 21555574.
- ↑ Oxenkrug G (2005). “Antioxidant effects of N-acetylserotonin: possible mechanisms and clinical implications”. 《Ann. N. Y. Acad. Sci.》 1053: 334–47. doi:10.1111/j.1749-6632.2005.tb00042.x. PMID 16179540.
- ↑ Gavazza MB.; Català A. (2004). “Protective effect of N-acetyl-serotonin on the nonenzymatic lipid peroxidation in rat testicular microsomes and mitochondria”. 《J. Pineal Res.》 37 (3): 153–60. doi:10.1111/j.1600-079x.2004.00150.x. PMID 15357659.
- ↑ Wölfler A.; Abuja PM.; Schauenstein K.; Liebmann PM. (1999). “N-acetylserotonin is a better extra- and intracellular antioxidant than melatonin”. 《FEBS Lett》 449 (2–3): 206–10. doi:10.1016/s0014-5793(99)00435-4. PMID 10338133.
- ↑ Peter Klemm; Markus Hecker; Hannelore Stockhausen; Chin Chen Wu; Christoph Thiemermann (Aug 1995). “Inhibition by N-acetyl-5-hydroxytryptamine of nitric oxide synthase expression in cultured cells and in the anaesthetized rat.”. 《Br J Pharmacol》 115 (7): 1175–1181. doi:10.1111/j.1476-5381.1995.tb15021.x. PMC 1908794. PMID 7582541.
- ↑ Perianayagam MC.; Oxenkrug GF.; Jaber BL. (2005). “Immune-modulating effects of melatonin, N-acetylserotonin, and N-acetyldopamine”. 《Ann. N. Y. Acad. Sci.》 1053: 386–93. doi:10.1111/j.1749-6632.2005.tb00046.x. PMID 16179544.
- ↑ 가 나 다 Oxenkrug GF (1999). “Antidepressive and antihypertensive effects of MAO-A inhibition: role of N-acetylserotonin. A review”. 《Neurobiology (Budapest, Hungary)》 7 (2): 213–24. PMID 10591054.
- ↑ 가 나 Oxenkrug GF (1997). “[N-acetylserotonin and hypotensive effect of MAO-A inhibitors]”. 《Voprosy Meditsinskoi Khimii》 (러시아어) 43 (6): 522–6. PMID 9503569.
- ↑ “N-Acetyl Serotonin”. DrugBank.
- v
- t
- e
| 주요 흥분계 / 억제계 |
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 생체 아민 |
| ||||||||
| 신경펩타이드 |
| ||||||||
| 엔도카나비노이드 |
| ||
|---|---|---|---|
| 신경스테로이드 |
| ||
| 뉴클레오사이드 |
|
|---|
| 콜린작동성계 |
|---|
| 기체전달물질 |
|---|
| 후보물질 |
|---|





