Fulvaleen
| Fulvaleen | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
 | ||||
Structuurformule van fulvaleen | ||||
 | ||||
Molecuulmodel van fulvaleen | ||||
| Algemeen | ||||
| Molecuulformule | C10H8 | |||
| IUPAC-naam | bicyclopentylideen-2,4,2',4'-tetraeen | |||
| Andere namen | bicyclopentadienylideen | |||
| Molmassa | 128,17052 g/mol | |||
| SMILES | C1=CC(=C2C=CC=C2)C=C1 | |||
| InChI | 1S/C10H8/c1-2-6-9(5-1)10-7-3-4-8-10/h1-8H | |||
| CAS-nummer | 91-12-3 | |||
| PubChem | 10908294 | |||
| Wikidata | Q415358 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | oranje | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Fulvaleen is een organische verbinding met als brutoformule C10H8. De verbinding is vooral van theoretisch belang als een van de eenvoudigste koolwaterstoffen met een geconjugeerd systeem die niet aromatisch is. Het komt voor als een oranje vloeistof.
Synthese
Vanwege het theoretische belang van de verbinding is lang naar een syntheseroute gezocht. In 1958 slaagde E.A. Matzner (werkend bij William von Eggers Doering) er voor het eerst in de verbinding te maken. Een eerdere poging in 1951 leidde per ongeluk tot de ontdekking van ferroceen.[1]
Fulvaleen kan bereid worden door reactie van cyclopentadieen met n-butyllithium, waardoor in eerste instantie het cyclopentadienyl-anion wordt gevormd. Dit anion wordt onder invloed van licht omgezet tot een intermediair radicaal, dat zeer snel dimeriseert. De gevormde binding wordt uiteindelijk geoxideerd tot een dubbele binding, waardoor fulvaleen ontstaat:
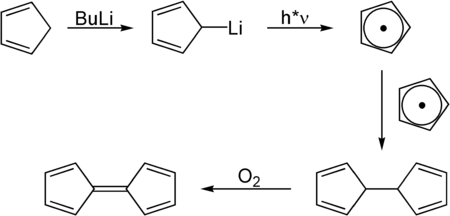
Synthese van fulvaleen
Structuur en eigenschappen
Fulvaleen bestaat uit twee cyclopentadieenringen, die via een dubbele binding met elkaar verbonden zijn. Dit zorgt ervoor dat beide ringen met elkaar geconjugeerd zijn. De molecule bezit een D2h-symmetrie.
Fulvaleen is een instabiel isomeer van de aromatische verbindingen naftaleen en azuleen. Het perchloorderivaat perchloorfulvaleen (C10Cl8) is - in tegenstelling tot fulvaleen - redelijk stabiel.[2] Het heterocyclische derivaat tetrathiafulvaleen gedraagt zich als een organische halfgeleider.
Fulvaleen als ligand
Fulvaleen vormt stabiele organometaalcomplexen.[3] De naam wordt dan meestal gekort tot Fv. In een aantal van deze fulvaleencomplexen (onder andere met ruthenium) kan de centrale dubbele binding reversibel gesplitst worden.[4]
Zie ook
- ↑ T. J. Kealy, P. L. Pauson (1951). A New Type of Organo-Iron Compound. Nature 168: 1039. DOI: 10.1038/1681039b0.
- ↑ (en) V. Mark (1973) - Perchlorofulvalene, Organic Syntheses, 5, p. 901. Gearchiveerd op 29 maart 2012.
- ↑ (en) K.B. Capps, G.D Whitener, A. Bauer, K.A. Abboud, I.M. Wasser, K.P.C. Vollhardt & C.D. Hoff (2002) - Synthesis and Crystal Structures of (Fulvalene)W2(SH)2(CO)6, (Fulvalene)W2(μ-S2)(CO)6, and (Fulvalene)W2(μ-S)(CO)6: Low Valent Tungsten Carbonyl Sulfide and Disulfide Complexes Stabilized by the Bridging Fulvalene Ligand[dode link], Inorganic Chemistry, 41, pp. 3212 -3217
- ↑ (en) R.J. Boese, K. Cammack, A.J. Matzger, K. Pflug, W.B. Tolman, K.P.C. Vollhardt & T.W. Weidman (1997) - Photochemistry of (Fulvalene)tetracarbonyldiruthenium and Its Derivatives: Efficient Light Energy Storage Devices, Journal of the American Chemistry Society, 119, p. 6757-6773. Gearchiveerd op 29 oktober 2019.











