Lithiumacetaat
| Lithiumacetaat | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
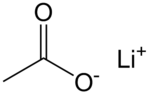 | ||||
Structuurformule van lithiumacetaat | ||||
 | ||||
Lithiumacetaat-kristallen (dihydraat) | ||||
| Algemeen | ||||
| Molecuulformule | C2H3LiO2 | |||
| IUPAC-naam | lithiumethanoaat | |||
| Molmassa | 65,98502 g/mol | |||
| SMILES | [Li+].CC(=O)[O-] | |||
| InChI | 1S/C2H4O2.Li/c1-2(3)4;/h1H3,(H,3,4);/q;+1/p-1 | |||
| CAS-nummer | 546-89-4 | |||
| EG-nummer | 208-914-3 | |||
| PubChem | 3474584 | |||
| Wikidata | Q416969 | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P264-P270-P301+P312-P330-P501 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | wit | |||
| Dichtheid | 1,26 g/cm³ | |||
| Smeltpunt | 286 °C | |||
| Oplosbaarheid in water | 450 g/L | |||
| Goed oplosbaar in | water | |||
| Geometrie en kristalstructuur | ||||
| Kristalstructuur | (watervrij) triklien (dihydraat) orthorombisch | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Lithiumacetaat is het lithiumzout van azijnzuur, met als brutoformule CH3COOLi. De stof komt voor als witte kristallen, die zeer goed oplosbaar zijn in water. Lithiumacetaat vormt ook een dihydraat.
Synthese
Lithiumacetaat kan bereid worden door reactie van lithiumhydroxide of lithiumcarbonaat met azijnzuur:[1]
Kristalstructuur
Lithiumacetaat kristalliseert als dihydraat uit in een orthorombische kristalstructuur. Het behoort tot de ruimtegroep Cmm2 en de parameters van de eenheidscel bedragen:[2]
- a = 6,86 Å
- b = 11,49 Å
- c = 6,59 Å
De watervrije kristallen bezitten een trikliene structuur en behoren tot ruimtegroep P1. De parameters van de eenheidscel bedragen:[3]
- a = 9,29 Å
- b = 12,13 Å
- c = 6,76 Å
- α = 101° 0'
- β = 100° 19'
- γ = 105° 5'
Toepassingen
Lithiumacetaat wordt in het laboratorium gebruikt als buffer bij de gel-elektroforese van DNA en RNA. Het bezit een lagere elektrische geleidbaarheid en bijgevolg is de warmteontwikkeling een stuk lager dan wanneer de klassieke TAE-buffer wordt gebruikt. Op die manier kan de aangelegde spanning verhoogd worden en kan de elektroforese versneld worden. Wanneer kleinere DNA-fragmenten dienen te worden gescheiden wordt echter gebruikgemaakt van een lithium- of natriumboraatbuffer, omwille van de hogere resolutie.
Verder wordt lithiumacetaat gebruikt als corrosie-inhibitor in polyfenylsulfideharsen en als katalysator bij de productie van polyesters, alkydharsen en acrylpolymeren.
Externe link
- (en) MSDS van lithiumacetaat
- ↑ (en) U. Wietelmann & R.J. Bauer (2005) - Lithium and Lithium compounds in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim
- ↑ (en) V. Amirthalingam & V.M. Padmanabhan (1958) - The crystal structure of lithium acetate dihydrate CH3COOLi · 2 H2O, Acta Cryst., 11, p. 896. Gearchiveerd op 3 juni 2018.
- ↑ (en) C. Saunderson & R.B. Ferguson (1961) - Crystal data for anhydrous lithium acetate, Acta Cryst., 14, p. 321. Gearchiveerd op 2 juni 2018.















