Nitrosylzwavelzuur
| Nitrosylzwavelzuur | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
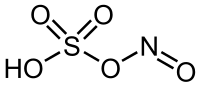 | |||||
Structuurformule van nitrosylzwavelzuur | |||||
| Algemeen | |||||
| Molecuulformule | NOHSO4 | ||||
| Molmassa | 127,08 g/mol | ||||
| CAS-nummer | 7782-78-7 | ||||
| Wikidata | Q419812 | ||||
| Beschrijving | Lichtgele kristallen | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H272 - H301 - H311 - H314 - H330 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P220 - P260 - P280 - P284 - P301+P310 - P305+P351+P338 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vast | ||||
| Kleur | lichtgeel | ||||
| Smeltpunt | 73,5 °C | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Nitrosylzwavelzuur, ook wel lodenkamerkristallen genoemd, wordt gevormd doordat er te weinig water wordt toegevoegd bij het oplossen van zwaveldioxide in de loden kamers van het lodenkamerproces. De kristallen vallen onder invloed van water uiteen in nitreuze dampen en zwavelzuur.
Nitrosylzwavelzuur wordt in essentie gevormd door de reactie tussen salpeterigzuur en zwavelzuur, of door reactie van zwaveldioxide met salpeterzuur:
Nitrosylzwavelzuur wordt in de scheikunde gebruikt om uit amines diazoniumzouten te maken. Het is commercieel beschikbaar als een oplossing in zwavelzuur.












