| ARR3 |
|---|
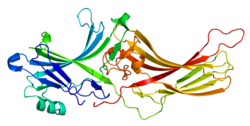 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 1XEH, 2A34 | | |
| Ідентифікатори |
|---|
| Символи | ARR3, ARRX, cArr, arrestin 3 retinal (X-arrestin), arrestin 3, MYP26 |
|---|
| Зовнішні ІД | OMIM: 301770 MGI: 2159617 HomoloGene: 3182 GeneCards: ARR3 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • phosphoprotein binding
• opsin binding
• GO:0001948, GO:0016582 protein binding
• G protein-coupled receptor binding
|
|---|
| Клітинна компонента | • photoreceptor inner segment
• цитоплазма
• photoreceptor outer segment
• синапс
|
|---|
| Біологічний процес | • regulation of protein phosphorylation
• ендоцитоз
• GO:0072468 сигнальна трансдукція
• зір
• відповідь на стимул
• G protein-coupled receptor internalization
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. X: 70.27 – 70.28 Mb | Хр. X: 99.65 – 99.66 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
ARR3 (англ. Arrestin 3) – білок, який кодується однойменним геном, розташованим у людей на X-хромосомі.[3] Довжина поліпептидного ланцюга білка становить 388 амінокислот, а молекулярна маса — 42 778[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MSKVFKKTSS | | NGKLSIYLGK | | RDFVDHVDTV | | EPIDGVVLVD | | PEYLKCRKLF |
| VMLTCAFRYG | | RDDLEVIGLT | | FRKDLYVQTL | | QVVPAESSSP | | QGPLTVLQER |
| LLHKLGDNAY | | PFTLQMVTNL | | PCSVTLQPGP | | EDAGKPCGID | | FEVKSFCAEN |
| PEETVSKRDY | | VRLVVRKVQF | | APPEAGPGPS | | AQTIRRFLLS | | AQPLQLQAWM |
| DREVHYHGEP | | ISVNVSINNC | | TNKVIKKIKI | | SVDQITDVVL | | YSLDKYTKTV |
| FIQEFTETVA | | ANSSFSQSFA | | VTPILAASCQ | | KRGLALDGKL | | KHEDTNLASS |
| TIIRPGMDKE | | LLGILVSYKV | | RVNLMVSCGG | | ILGDLTASDV | | GVELPLVLIH |
| PKPSHEAASS | | EDIVIEEFTR | | KGEEESQKAV | | EAEGDEGS |
Задіяний у такому біологічному процесі, як альтернативний сплайсинг.
Література
- Murakami A., Yajima T., Sakuma H., McLaren M.J., Inana G. (1993). X-arrestin: a new retinal arrestin mapping to the X chromosome. FEBS Lett. 334: 203—209. PMID 8224247 DOI:10.1016/0014-5793(93)81712-9
- Sakuma H., Inana G., Murakami A., Higashide T., McLaren M.J. (1996). Immunolocalization of X-arrestin in human cone photoreceptors. FEBS Lett. 382: 105—110. PMID 8612728 DOI:10.1016/0014-5793(96)00163-9
- Sakuma H., Murakami A., Fujimaki T., Inana G. (1998). Isolation and characterization of the human X-arrestin gene. Gene. 224: 87—95. PMID 9931451 DOI:10.1016/S0378-1119(98)00510-1
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Craft C.M., Whitmore D.H., Wiechmann A.F. (1994). Cone arrestin identified by targeting expression of a functional family. J. Biol. Chem. 269: 4613—4619. PMID 8308033
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:710 (англ.) . Процитовано 12 вересня 2017.
- ↑ UniProt, P36575 (англ.) . Архів оригіналу за 18 липня 2017. Процитовано 12 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |













