| MAP3K11 |
|---|
|
| Ідентифікатори |
|---|
| Символи | MAP3K11, MEKK11, MLK-3, MLK3, PTK1, SPRK, mitogen-activated protein kinase kinase kinase 11 |
|---|
| Зовнішні ІД | OMIM: 600050 MGI: 1346880 HomoloGene: 37618 GeneCards: MAP3K11 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • transferase activity
• nucleotide binding
• protein homodimerization activity
• mitogen-activated protein kinase kinase kinase binding
• kinase activity
• GO:0001948, GO:0016582 protein binding
• identical protein binding
• mitogen-activated protein kinase kinase binding
• ATP binding
• MAP kinase kinase kinase activity
• protein serine/threonine kinase activity
• protein kinase activity
• JUN kinase kinase kinase activity
• protein tyrosine kinase activity
|
|---|
| Клітинна компонента | • центросома
• мембрана
• центр організації мікротрубочок
• мікротрубочка
• цитоскелет
• цитоплазма
• внутрішньоклітинний
|
|---|
| Біологічний процес | • фосфорилювання
• positive regulation of JUN kinase activity
• смерть клітини
• positive regulation of JNK cascade
• positive regulation of neuron apoptotic process
• microtubule-based process
• проліферація
• protein autophosphorylation
• JNK cascade
• protein phosphorylation
• positive regulation of apoptotic process
• MAPK cascade
• peptidyl-tyrosine phosphorylation
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
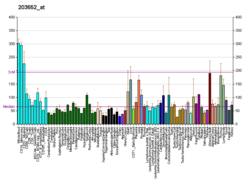 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. 11: 65.6 – 65.62 Mb | Хр. 19: 5.74 – 5.75 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
MAP3K11 (англ. Mitogen-activated protein kinase kinase kinase 11) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 11-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 847 амінокислот, а молекулярна маса — 92 688[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MEPLKSLFLK | | SPLGSWNGSG | | SGGGGGGGGG | | RPEGSPKAAG | | YANPVWTALF |
| DYEPSGQDEL | | ALRKGDRVEV | | LSRDAAISGD | | EGWWAGQVGG | | QVGIFPSNYV |
| SRGGGPPPCE | | VASFQELRLE | | EVIGIGGFGK | | VYRGSWRGEL | | VAVKAARQDP |
| DEDISVTAES | | VRQEARLFAM | | LAHPNIIALK | | AVCLEEPNLC | | LVMEYAAGGP |
| LSRALAGRRV | | PPHVLVNWAV | | QIARGMHYLH | | CEALVPVIHR | | DLKSNNILLL |
| QPIESDDMEH | | KTLKITDFGL | | AREWHKTTQM | | SAAGTYAWMA | | PEVIKASTFS |
| KGSDVWSFGV | | LLWELLTGEV | | PYRGIDCLAV | | AYGVAVNKLT | | LPIPSTCPEP |
| FAQLMADCWA | | QDPHRRPDFA | | SILQQLEALE | | AQVLREMPRD | | SFHSMQEGWK |
| REIQGLFDEL | | RAKEKELLSR | | EEELTRAARE | | QRSQAEQLRR | | REHLLAQWEL |
| EVFERELTLL | | LQQVDRERPH | | VRRRRGTFKR | | SKLRARDGGE | | RISMPLDFKH |
| RITVQASPGL | | DRRRNVFEVG | | PGDSPTFPRF | | RAIQLEPAEP | | GQAWGRQSPR |
| RLEDSSNGER | | RACWAWGPSS | | PKPGEAQNGR | | RRSRMDEATW | | YLDSDDSSPL |
| GSPSTPPALN | | GNPPRPSLEP | | EEPKRPVPAE | | RGSSSGTPKL | | IQRALLRGTA |
| LLASLGLGRD | | LQPPGGPGRE | | RGESPTTPPT | | PTPAPCPTEP | | PPSPLICFSL |
| KTPDSPPTPA | | PLLLDLGIPV | | GQRSAKSPRR | | EEEPRGGTVS | | PPPGTSRSAP |
| GTPGTPRSPP | | LGLISRPRPS | | PLRSRIDPWS | | FVSAGPRPSP | | LPSPQPAPRR |
| APWTLFPDSD | | PFWDSPPANP | | FQGGPQDCRA | | QTKDMGAQAP | | WVPEAGP |
Кодований геном білок за функціями належить до трансфераз, кіназ, серин/треонінових протеїнкіназ, фосфопротеїнів. Задіяний у такому біологічному процесі, як альтернативний сплайсинг. Білок має сайт для зв'язування з АТФ, нуклеотидами. Локалізований у цитоплазмі, цитоскелеті.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Leung I.W.L., Lassam N.J. (1998). Dimerization via tandem leucine zippers is essential for the activation of the mitogen-activated protein kinase kinase kinase, MLK-3. J. Biol. Chem. 273: 32408—32415. PMID 9829970 DOI:10.1074/jbc.273.49.32408
- Leung I.W.L., Lassam N.J. (2001). The kinase activation loop is the key to mixed lineage kinase-3 activation via both autophosphorylation and hematopoietic progenitor kinase 1 phosphorylation. J. Biol. Chem. 276: 1961—1967. PMID 11053428 DOI:10.1074/jbc.M004092200
- Vacratsis P.O., Phinney B.S., Gage D.A., Gallo K.A. (2002). Identification of in vivo phosphorylation sites of MLK3 by mass spectrometry and phosphopeptide mapping. Biochemistry. 41: 5613—5624. PMID 11969422 DOI:10.1021/bi016075c
- Swenson K.I., Winkler K.E., Means A.R. (2003). A new identity for MLK3 as an NIMA-related, cell cycle-regulated kinase that is localized near centrosomes and influences microtubule organization. Mol. Biol. Cell. 14: 156—172. PMID 12529434 DOI:10.1091/mbc.E02-02-0115
- Chadee D.N., Kyriakis J.M. (2004). MLK3 is required for mitogen activation of B-Raf, ERK and cell proliferation. Nat. Cell Biol. 6: 770—776. PMID 15258589 DOI:10.1038/ncb1152
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:6850 (англ.) . Архів оригіналу за 8 вересня 2015. Процитовано 8 вересня 2017.
- ↑ UniProt, Q16584 (англ.) . Архів оригіналу за 31 жовтня 2017. Процитовано 8 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |










