| TGM2 |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| Список кодів PDB | | 4PYG, 1KV3, 2Q3Z, 3LY6, 3S3J, 3S3P, 3S3S | | |
| Ідентифікатори |
|---|
| Символи | TGM2, G-ALPHA-h, GNAH, HEL-S-45, TG2, TGC, TG(C), transglutaminase 2, G(h), hTG2, tTG |
|---|
| Зовнішні ІД | OMIM: 190196 MGI: 98731 HomoloGene: 3391 GeneCards: TGM2 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • transferase activity
• acyltransferase activity
• protein-glutamine gamma-glutamyltransferase activity
• GO:0001948, GO:0016582 protein binding
• зв'язування з іоном металу
• GTP binding
• protein domain specific binding
|
|---|
| Клітинна компонента | • цитоплазма
• intrinsic component of plasma membrane
• гіалоплазма
• екзосома
• focal adhesion
• мітохондрія
• ендоплазматичний ретикулум
• клітинна мембрана
• GO:0005578 Позаклітинна матриця
• collagen-containing extracellular matrix
|
|---|
| Біологічний процес | • apoptotic cell clearance
• phospholipase C-activating G protein-coupled receptor signaling pathway
• salivary gland cavitation
• negative regulation of endoplasmic reticulum calcium ion concentration
• positive regulation of mitochondrial calcium ion concentration
• GO:0051357, GO:0051358, GO:0051359 peptide cross-linking
• positive regulation of cell adhesion
• branching involved in salivary gland morphogenesis
• positive regulation of inflammatory response
• positive regulation of I-kappaB kinase/NF-kappaB signaling
• positive regulation of cytosolic calcium ion concentration involved in phospholipase C-activating G protein-coupled signaling pathway
• isopeptide cross-linking via N6-(L-isoglutamyl)-L-lysine
• positive regulation of apoptotic process
• protein homooligomerization
• positive regulation of smooth muscle cell proliferation
• blood vessel remodeling
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
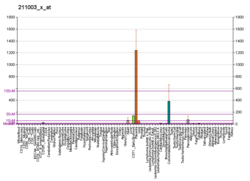
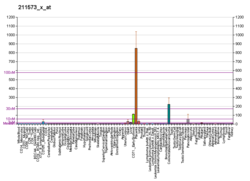
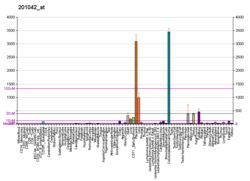 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_004613
NM_198951
NM_001323316
NM_001323317
NM_001323318 |
| |
|---|
| RefSeq (білок) | | NP_001310245
NP_001310246
NP_001310247
NP_004604
NP_945189 |
| |
|---|
| Локус (UCSC) | Хр. 20: 38.13 – 38.17 Mb | Хр. 2: 157.96 – 157.99 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
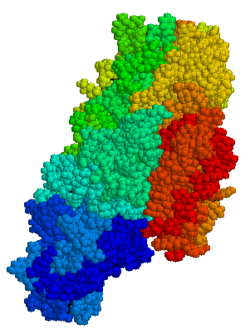
TGM2 (англ. Transglutaminase 2) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 20-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 687 амінокислот, а молекулярна маса — 77 329[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MAEELVLERC | | DLELETNGRD | | HHTADLCREK | | LVVRRGQPFW | | LTLHFEGRNY |
| EASVDSLTFS | | VVTGPAPSQE | | AGTKARFPLR | | DAVEEGDWTA | | TVVDQQDCTL |
| SLQLTTPANA | | PIGLYRLSLE | | ASTGYQGSSF | | VLGHFILLFN | | AWCPADAVYL |
| DSEEERQEYV | | LTQQGFIYQG | | SAKFIKNIPW | | NFGQFEDGIL | | DICLILLDVN |
| PKFLKNAGRD | | CSRRSSPVYV | | GRVVSGMVNC | | NDDQGVLLGR | | WDNNYGDGVS |
| PMSWIGSVDI | | LRRWKNHGCQ | | RVKYGQCWVF | | AAVACTVLRC | | LGIPTRVVTN |
| YNSAHDQNSN | | LLIEYFRNEF | | GEIQGDKSEM | | IWNFHCWVES | | WMTRPDLQPG |
| YEGWQALDPT | | PQEKSEGTYC | | CGPVPVRAIK | | EGDLSTKYDA | | PFVFAEVNAD |
| VVDWIQQDDG | | SVHKSINRSL | | IVGLKISTKS | | VGRDEREDIT | | HTYKYPEGSS |
| EEREAFTRAN | | HLNKLAEKEE | | TGMAMRIRVG | | QSMNMGSDFD | | VFAHITNNTA |
| EEYVCRLLLC | | ARTVSYNGIL | | GPECGTKYLL | | NLNLEPFSEK | | SVPLCILYEK |
| YRDCLTESNL | | IKVRALLVEP | | VINSYLLAER | | DLYLENPEIK | | IRILGEPKQK |
| RKLVAEVSLQ | | NPLPVALEGC | | TFTVEGAGLT | | EEQKTVEIPD | | PVEAGEEVKV |
| RMDLLPLHMG | | LHKLVVNFES | | DKLKAVKGFR | | NVIIGPA |
Кодований геном білок за функціями належить до трансфераз, ацилтрансфераз, фосфопротеїнів. Задіяний у таких біологічних процесах, як ацетилювання, альтернативний сплайсинг. Білок має сайт для зв'язування з іонами металів, іоном кальцію.
Література
- Fraij B.M., Gonzales R.A. (1996). A third human tissue transglutaminase homologue as a result of alternative gene transcripts. Biochim. Biophys. Acta. 1306: 63—74. PMID 8611626 DOI:10.1016/0167-4781(95)00219-7
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Pinkas D.M., Strop P., Brunger A.T., Khosla C. (2007). Transglutaminase 2 undergoes a large conformational change upon activation. PLoS Biol. 5: E327—E327. PMID 18092889 DOI:10.1371/journal.pbio.0050327
- Fraij B.M., Birckbichler P.J., Patterson M.K. Jr., Lee K.N., Gonzales R.A. (1992). A retinoic acid-inducible mRNA from human erythroleukemia cells encodes a novel tissue transglutaminase homologue. J. Biol. Chem. 267: 22616—22623. PMID 1358880
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:11778 (англ.) . Архів оригіналу за 15 листопада 2015. Процитовано 12 вересня 2017.
- ↑ UniProt, P21980 (англ.) . Архів оригіналу за 25 вересня 2017. Процитовано 12 вересня 2017.
Див. також
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
















